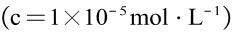化学工艺流程专题突破策略学案
化学工艺流程专题突破学案
一. 课前真题回顾(每题计时完成)
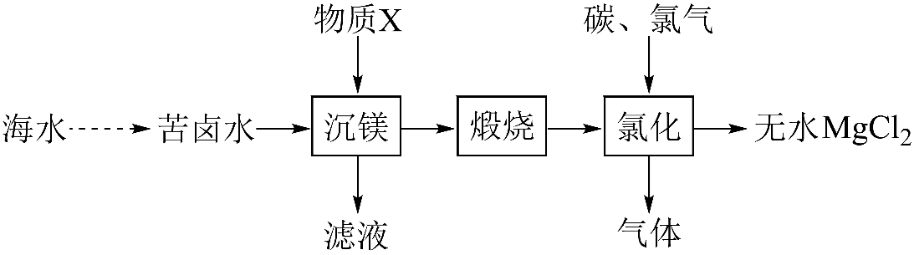
1.【2021·湖南真题】一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是
A.物质X常选用生石灰
B.工业上常用电解熔融制备金属镁
C.“氯化”过程中发生的反应为
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水
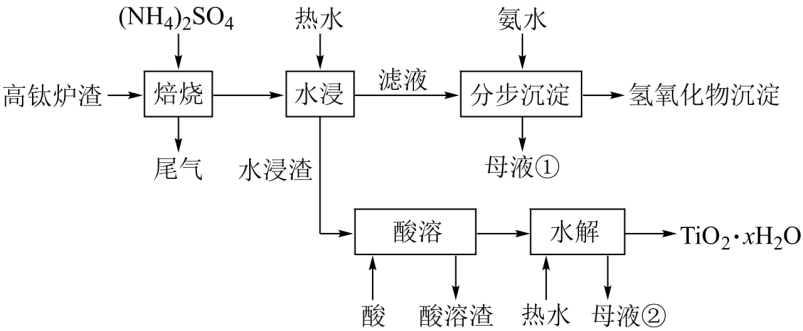
2.【2021全国乙卷26题】磁选后的炼铁高钛炉渣,主要成分有TiO2、SiO2、Al2O3、MgO、CaO以及少量的Fe2O3。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 | Fe3+ | Al3+ | Mg2+ | Ca2+ |
开始沉淀的pH | 2.2 | 3.5 | 9.5 | 12.4 |
| 3.2 | 4.7 | 11.1 | 13.8 |
回答下列问题:
(1)“焙烧”中,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,写出Al2O3转化为NH4Al(SO4)2的化学方程式_________________________________________________。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次析出的金属离子是_________________。
(3)“母液①"中Mg2+浓度为_______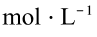
(4)“水浸渣”在160℃“酸溶”最适合的酸是____________。“酸溶渣”的成分是____________、____________。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO2·xH2O沉淀,该反应的离子方程式是_________________________________________________。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得______________,循环利用。
3. 【2021辽宁卷16】从钒铬锰矿渣(主要成分为V2O5

已知:pH较大时,二价锰在空气中易被氧化。回答下列问题:
(1)Cr元素位于元素周期表第_______周期_______族。
(2)用FeCl3
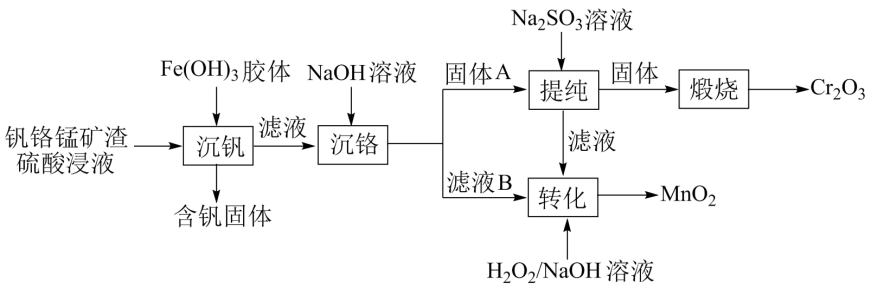
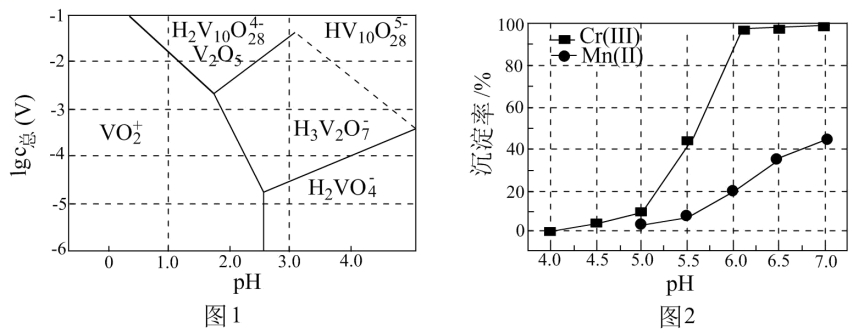
(3)常温下,各种形态五价钒粒子总浓度的对数[lgc总(V)]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中c总(V) = 0.01mol/L,“沉钒”过程控制pH = 3.0,则与胶体共沉降的五价钒粒子的存在形态为__________(填化学式)。
(4)某温度下,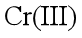
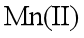
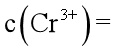

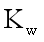
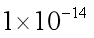
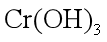
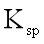
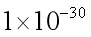
(5)“转化”过程中生成MnO2的离子方程式为___________________________________。
(6)“提纯”过程中Na2S2O3的作用为___________________________________。
4.【2019新课标Ⅰ卷】硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
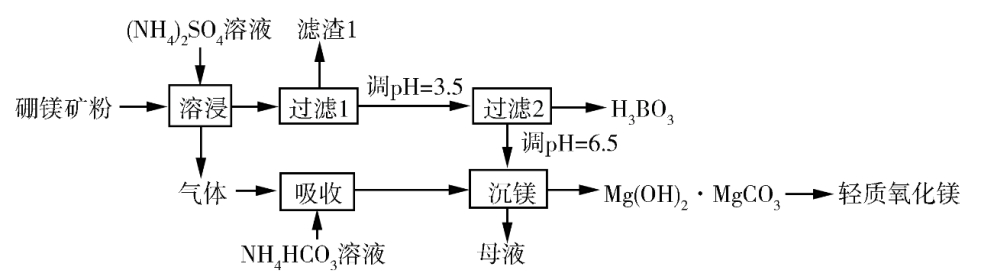
(1)在95 ℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为___________________________。
(2)“滤渣1”的主要成分有_________。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是_________。
(3)根据H3BO3的解离反应:H3BO3+H2O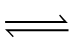
(4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为____________________________,母液经加热后可返回___________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是___________________________。
二.专题课后练习
1.尝试利用下列材料命制一道化学工艺流程题:
利用某含铬废液【含较低浓度浓度的Na2Cr2O7、Fe2(SO4)3】制备K2Cr2O7流程如下:
(1)用NaOH溶液调pH至3.6,产生红褐色沉淀,过滤;
(2)向滤液中加入Na2SO3,一定操作后分离出Na2SO4・10H2O;
(3)将分离出Na2SO4・10H2O后的溶液调pH约为5,得到Cr(OH)3沉淀;
(4)在KOH存在条件下,向Cr(OH)3中加入足量H2O2溶液,得到黄色溶液;
(5)向黄色溶液中加入物质A后,溶液变为橙红色,一定操作后得到K2Cr2O7固体;
(6)测定K2Cr2O7,固体的纯度。
(建议设问:(1)原料的处理阶段时的条件控制;(2)反应方程式的书写;(3)pH与沉淀溶解平衡结合的计算题;(4)反应方程式的书写;(5)分离提纯操作;(6)纯度计算)
计时完成下列各题:
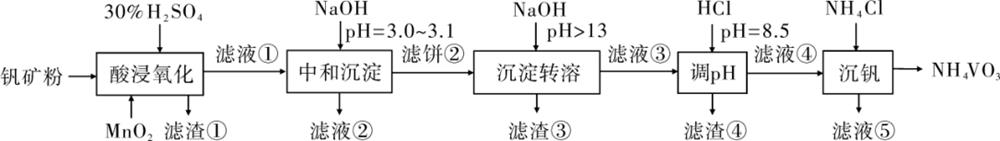
2.【2020新课标Ⅰ卷26题】钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是________________________________。
(2)“酸浸氧化”中,VO+和VO2+被氧化成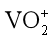
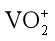
(3)“中和沉淀”中,钒水解并沉淀为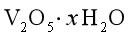
(4)“沉淀转溶”中,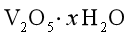
(5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是_________________________。
(6)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是_________________________。
3. 综合利用炼锌矿渣(主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4)获得3种金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如下:
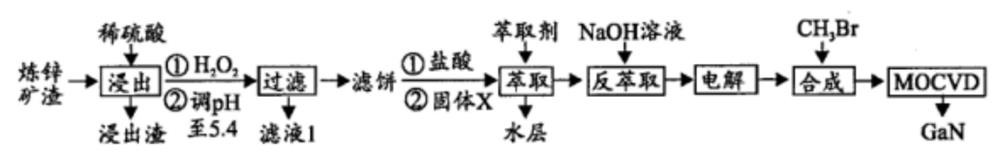
已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH见表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表2。
表1金属离子浓度及开始沉淀的pH
金属离子 | 浓度(mol·L-1) | 开始沉淀pH |
Fe2+ | 1.0×10-3 | 8.0 |
Fe3+ | 4.0×10-2 | 1.7 |
Zn2+ | 1.5 | 5.5 |
Ga3+ | 3.0×10-3 | 3.0 |
表2金属离子的萃取率
金属离子 | 萃取率(%) |
Fe2+ | 0 |
Fe3+ | 99 |
Zn2+ | 0 |
Ga3+ | 97-98.5 |
(1)Ga2(Fe2O4)3中Ga的化合价为__________________,“浸出”时其发生反应的离子方程式为____________。
(2)滤液1中可回收利用的物质是__________________,滤饼的主要成分是__________________;萃取前加入的固体X为__________________。
(3)Ga与Al同主族,化学性质相似。反萃取后,镓的存在形式为__________ (填化学式)。
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以NaOH溶液为电解液,阴极的电极反应为______________________________。
(5)GaN可采用MOCVD (金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为________________________。
(6)滤液1中残余的Ga3+的浓度为__________________ mol·L-1 (写出计算过程)。